【
儀表網 研發快訊】近日,上海交通大學變革性分子前沿科學中心孫浩課題組在取得了重要研究進展,其揭示了含氟電解液添加劑在鈉-氯氣電池中的作用機制,相關研究成果以“Unveiling cathode catalysis of fluorinated electrolyte additives for high-performance Na-Cl2 batteries”為題發表于Natl. Sci. Rev.(國家科學評論),第一作者為變革性分子前沿科學中心博士生徐秋晨和唐姍姍,通訊作者為孫浩副教授和趙孝菊博士。本工作得到了國家自然科學基金、中央高校基本科研業務費專項資金、上海交通大學變革性分子前沿科學中心、張江高等研究院的大力支持。
可充電鈉-氯氣(Na-Cl2)電池因其高能量密度和低成本等優勢而成為高性能儲能技術的有力候選者。該電池通常采用由氯化鋁(AlCl3)和亞硫酰氯(SOCl2)構成的氯鋁酸鹽電解液,為了提升電池的循環穩定性,常在電解液中引入雙氟磺酰亞胺鈉(NaFSI)等含氟添加劑,通常認為這種添加劑會在金屬表面分解形成氟化鈉,構成固態電解質界面層(SEI),從而抑制鈉金屬和電解液的副反應,延長電池循環壽命。然而,這一作用機制尚未得到充分驗證,含氟電解液添加劑在Na-Cl2電池中的真實作用亟需厘清,以有效指導可充電Na-Cl2電池的材料設計和性能提升。
鑒于此,上海交通大學變革性分子前沿科學中心副教授、張江高等研究院入駐科學家、化學化工學院孫浩課題組開展了系統研究,發現含氟電解液添加劑在電池負極側的作用有限,而是在正極側通過化學反應原位生成氟化鋁(AlF3)催化劑,進而顯著提升了NaCl/Cl2的氧化還原反應動力學。基于該機理,提出了正極直接負載高性能催化劑策略,顯著提升了電池的倍率和循環性能。
圖1. FSI?陰離子在傳統鈉金屬電池與Na-Cl2電池中的作用機制示意圖
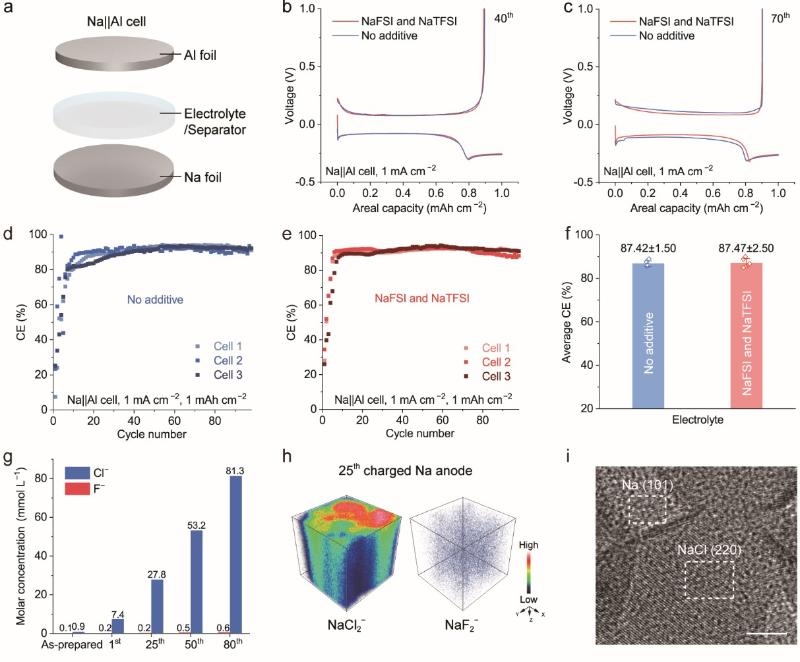
通過電解液成分分析,研究團隊發現電解液中的FSI?陰離子與AlCl3發生自發化學反應,導致S–F鍵斷裂并生成AlCl3F−離子。Na||Al半電池測試結果進一步顯示,引入含氟添加劑并未顯著提升鈉金屬的沉積/剝離效率。通過飛行時間
二次離子質譜與低溫透射電鏡等表征方法對負極界面組分的深入分析顯示,SEI主要組分為氯化鈉,而氟化鈉信號幾乎無法檢出。上述結果表明含氟添加劑對負極側的作用并非影響電池性能的主要因素。
圖2. 含氟電解液添加劑調控的負極電化學性能與界面化學
對循環后正極的表征結果表明,AlCl3F−在循環過程中會逐漸演化,最終轉化為AlF3,并呈現出與NaCl交錯分布的特點,這表明AlF3對NaCl的氧化反應具有催化作用。機理研究證實,AlF3作為一種強路易斯酸,能夠有效促進電子從NaCl向碳基底的轉移,從而顯著降低NaCl氧化生成Cl2的反應能壘,極大提升正極反應動力學。
圖3. AlF3在正極上的分布與催化機制
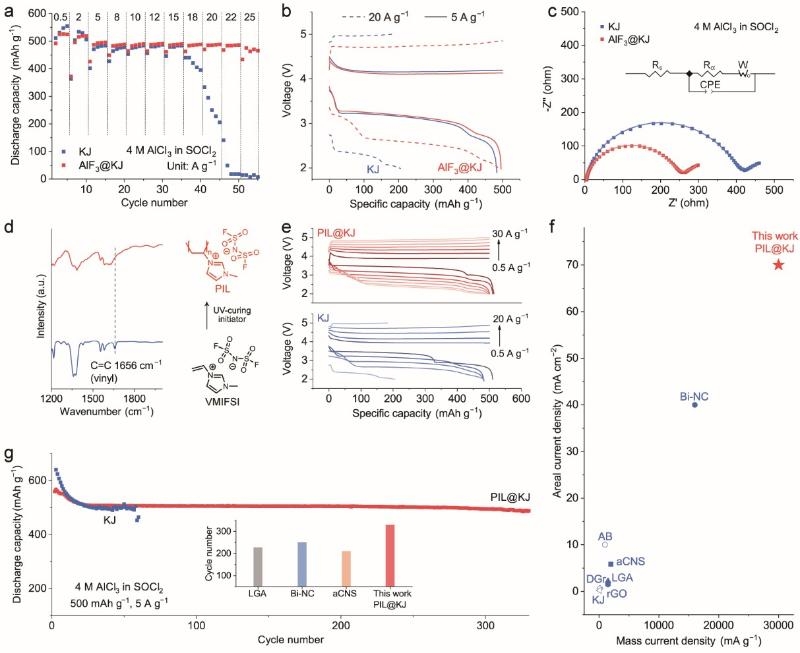
基于上述機理認知,研究團隊進一步提出兩種電池性能優化策略:一是直接將AlF3粉末摻入正極,實現了高達25 A g−1的倍率性能;二是設計并合成了一種含有FSI−陰離子的聚離子液體(PIL)作為正極催化材料。PIL優異的成膜性促進了AlF3的均勻分布,從而調控了NaCl的生長形貌,防止電極鈍化,最終使電池在30 A g−1的超高電流密度下穩定運行,其性能遠超當前最先進的Na-Cl2及Li-Cl2電池。
圖4. 通過正極直接負載催化劑提升倍率與循環性能
綜上所述,本工作闡明了含氟電解液添加劑在Na-Cl2電池中的獨特作用機制,即并非在負極形成固態電解質中間相以保護負極,而是通過與電解液發生自發化學反應,在正極上原位生成AlF3催化劑,從而提升了NaCl/Cl2氧化還原反應動力學和可逆性。該機制為發展高功率密度、長壽命金屬-氯氣電池提供了關鍵的理論依據,并且提供了一種將負極保護性添加劑轉變為正極催化劑的新思路,為發展高倍率、長循環轉化型電池提供了理論和實驗依據。






所有評論僅代表網友意見,與本站立場無關。